กรดไนตริก, (HNO 3), ไม่มีสี, เป็นไอ, และของเหลวที่มีฤทธิ์กัดกร่อนสูง (จุดเยือกแข็ง −42 ° C [−44 ° F], จุดเดือด 83 ° C [181 ° F]) ซึ่งเป็นรีเอเจนต์ทางห้องปฏิบัติการทั่วไปและสำคัญ สารเคมีอุตสาหกรรมสำหรับการผลิตปุ๋ยและวัตถุระเบิด มันเป็นพิษและอาจทำให้เกิดแผลไหม้อย่างรุนแรง
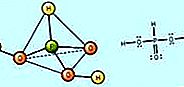
oxyacid: กรดไนตริกและเกลือไนเตรต
กรดไนตริก HNO3 เป็นที่รู้จักกันในหมู่นักเล่นแร่แปรธาตุของศตวรรษที่ 8 ว่า "aqua fortis" (น้ำแรง) มันถูกสร้างขึ้น
การเตรียมและการใช้กรดไนตริกเป็นที่รู้กันโดยนักเล่นแร่แปรธาตุตอนต้น กระบวนการห้องปฏิบัติการทั่วไปที่ใช้เป็นเวลาหลายปีกำหนดให้นักเคมีชาวเยอรมันโยฮันน์รูดอล์ฟกลูเบอร์ (1648) ประกอบด้วยโพแทสเซียมไนเตรตร้อนกับกรดซัลฟิวริกเข้มข้น ใน 1,776 Antoine-Laurent Lavoisier แสดงให้เห็นว่ามันมีออกซิเจนและใน 1,816 Joseph-Louis Gay-Lussac และ Claude-Louis Berthollet สร้างองค์ประกอบทางเคมีของมัน
วิธีการหลักในการผลิตกรดไนตริกคือตัวเร่งปฏิกิริยาออกซิเดชันของแอมโมเนีย ในวิธีการที่พัฒนาโดยวิลเฮล์มออสต์วาลด์นักเคมีชาวเยอรมันในปี 1901 ก๊าซแอมโมเนียถูกออกซิไดซ์อย่างต่อเนื่องเพื่อไนตริกออกไซด์และไนโตรเจนไดออกไซด์โดยอากาศหรือออกซิเจนเมื่อมีตัวเร่งปฏิกิริยาแพลตตินัม ไนโตรเจนไดออกไซด์จะถูกดูดซึมในน้ำเพื่อสร้างกรดไนตริก สารละลายกรดในน้ำที่เกิดขึ้น (ประมาณ 50–70 เปอร์เซ็นต์โดยกรดน้ำหนัก) สามารถถูกทำให้แห้งโดยการกลั่นด้วยกรดซัลฟูริก
กรดไนตริกสลายตัวเป็นน้ำไนโตรเจนไดออกไซด์และออกซิเจนก่อตัวเป็นสารละลายสีเหลืองน้ำตาล เป็นกรดแก่ไอออนไนซ์อย่างสมบูรณ์ในไฮโดรเนียม (H 3 O +) และไนเตรต (NO 3 -) ไอออนในสารละลายน้ำและสารออกซิไดซ์ที่ทรงพลัง (หนึ่งที่ทำหน้าที่เป็นตัวรับอิเล็กตรอนในปฏิกิริยาลดออกซิเดชัน) ปฏิกิริยาที่สำคัญหลายประการของกรดไนตริกคือการทำปฏิกิริยากับแอมโมเนียให้เป็นแอมโมเนียมไนเตรตซึ่งเป็นองค์ประกอบสำคัญของปุ๋ย ไนเตรทของกลีเซอรอลและโทลูอีนทำให้เกิดไนโตรกลีเซอรีนและทรินทรินโตลูอีน (TNT) ตามลำดับ; การเตรียมไนโตรเซลลูโลส และออกซิเดชันของโลหะกับออกไซด์หรือไนเตรตที่เกี่ยวข้อง




![พระราชบัญญัติควิเบกบริเตนใหญ่ [1774] พระราชบัญญัติควิเบกบริเตนใหญ่ [1774]](https://images.thetopknowledge.com/img/politics-law-government/5/quebec-act-great-britain-1774.jpg)



