แผนภาพแสดงสถานะกราฟแสดงเงื่อนไขการ จำกัด สำหรับเฟสของแข็งของเหลวและก๊าซของสารเดี่ยวหรือส่วนผสมของสารในขณะที่การเปลี่ยนแปลงของความดันและอุณหภูมิหรือในการรวมกันของตัวแปรอื่น ๆ เช่นการละลายและอุณหภูมิ รูปแสดงไดอะแกรมเฟสทั่วไปสำหรับระบบหนึ่งองค์ประกอบ (เช่นที่ประกอบด้วยสารบริสุทธิ์เดียว) เส้นโค้งที่ได้รับจากการวัดที่ทำจากแรงกดดันและอุณหภูมิที่หลากหลาย ณ จุดใด ๆ ในพื้นที่ที่คั่นด้วยเส้นโค้งความดันและอุณหภูมิอนุญาตให้มีเฟสเดียว (ของแข็งของเหลวหรือก๊าซ) และการเปลี่ยนแปลงของอุณหภูมิและความดันจนถึงจุดบนเส้นโค้งจะไม่เปลี่ยนแปลงเฟสนี้. ที่จุดใด ๆ บนเส้นโค้งอุณหภูมิและความดันอนุญาตให้มีสองขั้นตอนอยู่ในสมดุล: ของแข็งและของเหลวของแข็งและไอหรือของเหลวและไอ ตัวอย่างเช่นเส้นที่ลากสำหรับการแปรผันตามอุณหภูมิของความดันไอสำหรับของเหลวนั้นเป็นขอบเขตระหว่างของเหลวกับไอ ไอเท่านั้นที่มีอยู่ในสายแรงดันต่ำและอุณหภูมิสูงในขณะที่สารต้องเป็นของเหลวที่ด้านแรงดันสูงและอุณหภูมิต่ำ ของเหลวและไอมีอยู่ด้วยกันที่อุณหภูมิและความดันที่สอดคล้องกับจุดบนเส้น ในสถานที่ที่เส้นนี้หายไปเรียกว่าจุดวิกฤติของเหลวและไอของมันจะแยกไม่ออก ตามเส้นแบ่งระหว่างของเหลวและของแข็งอุณหภูมิหลอมละลายสำหรับแรงกดดันที่แตกต่างกันสามารถพบได้ จุดเชื่อมต่อของสามโค้งเรียกว่าจุดสามจุดแสดงให้เห็นถึงเงื่อนไขที่ไม่ซ้ำกันซึ่งทั้งสามขั้นตอนอยู่ในสมดุลด้วยกัน แผนภาพเฟสสำหรับสององค์ประกอบมักจะแสดงเส้นโค้งหลอมละลายบนแผนภาพองค์ประกอบของอุณหภูมิ
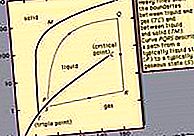
ของเหลว: แผนภาพเฟสของสารบริสุทธิ์
เมื่ออุณหภูมิและความดันของสารบริสุทธิ์ได้รับการแก้ไขสถานะของสารจะคงที่เช่นกัน นี่คือตัวอย่าง
เฟสไดอะแกรมมีความเฉพาะสำหรับแต่ละสารและของผสม สารผสมที่ซับซ้อนอาจต้องการไดอะแกรมเฟสสามมิติซึ่งสามารถแสดงเป็นสองมิติผ่านการใช้มุมมอง เฟสไดอะแกรมถูกนำมาใช้อย่างกว้างขวางในการศึกษาสมดุลของแร่ธาตุที่เกี่ยวข้องกับเงื่อนไขการก่อตัวของหินและแร่ธาตุในโลก พวกเขายังมีค่าเมื่อออกแบบอุปกรณ์อุตสาหกรรมและแสวงหาเงื่อนไขที่เหมาะสมสำหรับกระบวนการผลิตและในการกำหนดความบริสุทธิ์ของสาร