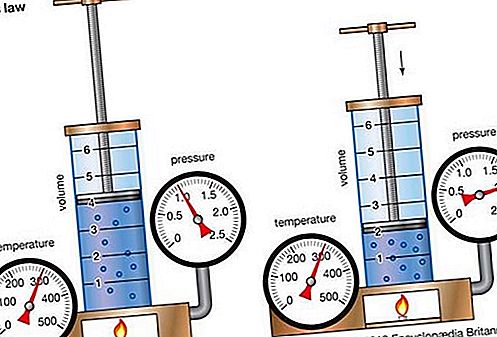
กฎของ Boyleหรือที่เรียกว่ากฎหมายของ Mariotteความสัมพันธ์ที่เกี่ยวข้องกับการบีบอัดและการขยายตัวของก๊าซที่อุณหภูมิคงที่ ความสัมพันธ์เชิงประจักษ์นี้จัดทำขึ้นโดยนักฟิสิกส์ Robert Boyle ในปี ค.ศ. 1662 กล่าวว่าแรงดัน (p) ของปริมาณก๊าซที่กำหนดนั้นแปรผกผันกับปริมาตร (v) ที่อุณหภูมิคงที่ คือในรูปแบบสมการ pv = k ค่าคงที่ ความสัมพันธ์ถูกค้นพบโดยนักฟิสิกส์ชาวฝรั่งเศส Edme Mariotte (1676)
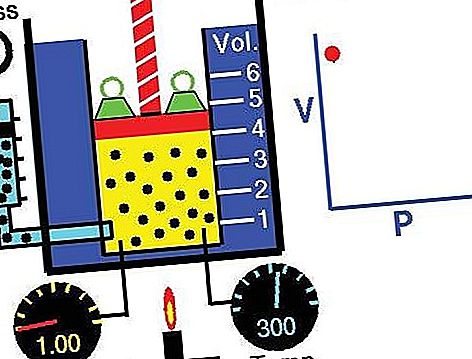
กฎหมายสามารถได้มาจากทฤษฎีจลน์ของแก๊สโดยสมมติว่าเป็นก๊าซอุดมคติ (อุดมคติ) (ดูก๊าซสมบูรณ์) ก๊าซจริงปฏิบัติตามกฎของ Boyle ที่ความดันต่ำพอสมควรถึงแม้ว่าผลิตภัณฑ์ pv จะลดลงเล็กน้อยที่ความกดดันสูงกว่าซึ่งก๊าซเริ่มจากพฤติกรรมในอุดมคติ