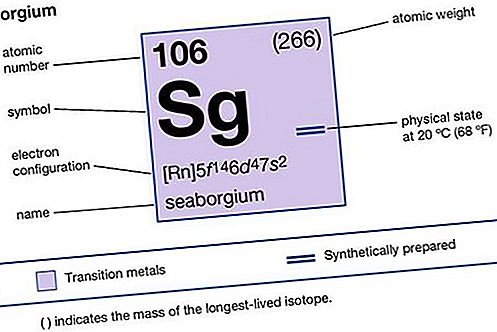
การแปรรูปแมกนีเซียมการเตรียมแร่แมกนีเซียมเพื่อใช้ในผลิตภัณฑ์ต่าง ๆ

แมกนีเซียม (Mg) เป็นโลหะสีขาวเงินที่มีลักษณะคล้ายกับอลูมิเนียม แต่มีน้ำหนักน้อยกว่าหนึ่งในสาม ด้วยความหนาแน่นเพียง 1.738 กรัมต่อลูกบาศก์เซนติเมตรมันเป็นโลหะโครงสร้างที่เบาที่สุดที่รู้จัก มันมีโครงสร้างผลึกรูปหกเหลี่ยมแบบปิดแน่น (hcp) ดังนั้นเช่นเดียวกับโลหะส่วนใหญ่ของโครงสร้างนี้มันขาดความเหนียวเมื่อทำงานที่อุณหภูมิต่ำกว่า นอกจากนี้ในรูปแบบบริสุทธิ์มันไม่มีความแข็งแรงเพียงพอสำหรับการใช้งานโครงสร้างส่วนใหญ่ อย่างไรก็ตามการเพิ่มองค์ประกอบผสมนั้นช่วยปรับปรุงคุณสมบัติของมันให้กว้างขึ้นซึ่งมีการใช้กันอย่างแพร่หลายโดยเฉพาะอย่างยิ่งที่น้ำหนักเบาและความแข็งแรงสูง
แมกนีเซียมมีปฏิกิริยารุนแรงกับออกซิเจนที่อุณหภูมิสูง สูงกว่า 645 ° C (1,190 ° F) ในอากาศแห้งมันเผาไหม้ด้วยแสงสีขาวสว่างและความร้อนจัด ด้วยเหตุนี้ผงแมกนีเซียมจึงถูกใช้ในดอกไม้ไฟ ที่อุณหภูมิห้องฟิล์มที่มีความเสถียรของแมกนีเซียมไฮดรอกไซด์ชนิดไม่ละลายน้ำจะเกิดขึ้นบนพื้นผิวโลหะป้องกันการกัดกร่อนในบรรยากาศส่วนใหญ่ ในฐานะที่เป็นสารตั้งต้นที่แข็งแกร่งซึ่งสร้างสารประกอบที่เสถียรด้วยคลอรีนออกซิเจนและกำมะถันแมกนีเซียมมีการใช้งานด้านโลหะหลายอย่างเช่นในการผลิตไทเทเนียมจากไทเทเนียมเตตระคลอไรด์และในการกำจัดกำมะถันของเหล็กเตาหลอมเหล็ก ปฏิกิริยาทางเคมีของมันยังเห็นได้ชัดในสารประกอบแมกนีเซียมที่มีการใช้กันอย่างแพร่หลายในอุตสาหกรรมการแพทย์และการเกษตร
ประวัติศาสตร์
แมกนีเซียมนั้นได้มาจากชื่อของแมกเนไซท์ซึ่งเป็นแร่แมกนีเซียมคาร์บอเนตและแร่ธาตุนี้ได้ถูกกล่าวถึงว่าเป็นชื่อของ Magnesite ที่พบในแมกนีเซียซึ่งเป็นเขตในภูมิภาคกรีกโบราณของเทสซา นักเคมีชาวอังกฤษฮัมฟรีย์เดวี่กล่าวกันว่ามีการรวมตัวกันของแมกนีเซียมใน 2351 โดยอิเล็กโทรไลต์แมกนีเซียมซัลเฟตชื้นด้วยการใช้ปรอทเป็นแคโทด อย่างไรก็ตามแมกนีเซียมโลหะแรกถูกผลิตขึ้นในปี 1828 โดยนักวิทยาศาสตร์ชาวฝรั่งเศส A.-A.-B Bussy งานของเขาเกี่ยวข้องกับการลดแมกนีเซียมคลอไรด์ที่หลอมเหลวด้วยโพแทสเซียมโลหะ ในปี 1833 Michael Faraday นักวิทยาศาสตร์ชาวอังกฤษเป็นคนแรกที่ผลิตแมกนีเซียมด้วยกระแสไฟฟ้าของแมกนีเซียมคลอไรด์ที่หลอมเหลว การทดลองของเขาถูกทำซ้ำโดยนักเคมีชาวเยอรมัน Robert Bunsen
การผลิตภาคอุตสาหกรรมที่ประสบความสำเร็จครั้งแรกเริ่มขึ้นในประเทศเยอรมนีในปีพ. ศ. 2429 โดยอลูมิเนียมและแม็กนีเซียมแฟบริคเฮเมลินเกน ต่อมา Hemelingen ได้กลายเป็นส่วนหนึ่งของอุตสาหกรรมที่ซับซ้อน IG Farbenindustrie ซึ่งในช่วงทศวรรษที่ 1920 และ 30 ได้มีการพัฒนากระบวนการผลิตแมกนีเซียมคลอไรด์ที่หลอมละลายจำนวนมากและโดยพื้นฐานแล้วเป็นที่รู้จักกันในนามกระบวนการ IG Farben สำหรับอิเล็กโทรไลต์ผลิตภัณฑ์นี้กับโลหะแมกนีเซียมและคลอรีน การมีส่วนร่วมอื่น ๆ ของ IG Farben คือการพัฒนาโลหะผสมที่หล่อและอ่อนได้จำนวนมากฟลักซ์การกลั่นและการป้องกันผลิตภัณฑ์แมกนีเซียมที่ทำขึ้นและการใช้งานเครื่องบินและรถยนต์จำนวนมาก ในช่วงสงครามโลกครั้งที่สอง บริษัท Dow Chemical แห่งสหรัฐอเมริกาและแมกนีเซียม Elektron Limited ของสหราชอาณาจักรเริ่มลดแมกนีเซียมด้วยไฟฟ้าจากน้ำทะเลที่สูบจากอ่าว Galveston, Texas และทะเลเหนือที่ Hartlepool ประเทศอังกฤษ ในเวลาเดียวกันในออนแทรีโอแคนาดากระบวนการ LM Pidgeon ของการลดความร้อนแมกนีเซียมออกไซด์ด้วยซิลิกอนในการตอบโต้การยิงจากภายนอกได้รับการแนะนำ
หลังจากสงครามการใช้งานทางทหารสูญเสียความโดดเด่น Dow Chemical ขยายตลาดพลเรือนโดยการพัฒนาผลิตภัณฑ์ที่ทำขึ้นเทคโนโลยี photoengraving และระบบการรักษาพื้นผิว การสกัดยังคงขึ้นอยู่กับกระแสไฟฟ้าและการลดความร้อน ในกระบวนการเหล่านี้ได้ทำการปรับแต่งเช่นความร้อนภายในของ retorts (กระบวนการ Magnetherm ที่นำมาใช้ในประเทศฝรั่งเศสในปี 1961) การสกัดจาก prills แมกนีเซียมคลอไรด์แห้ง (แนะนำโดย บริษัท นอร์เวย์ Norsk Hydro ในปี 1974) และการปรับปรุงเทคโนโลยีเซลล์ไฟฟ้าจาก ประมาณ 1970
ในปี 2019 จีนผลิตแมกนีเซียมประมาณร้อยละ 85 ของโลกและรัสเซียคาซัคสถานอิสราเอลและบราซิลผลิตส่วนที่เหลือมาก
แร่และวัตถุดิบ
ธาตุที่แปดที่มีมากที่สุดในธรรมชาติแมกนีเซียมถือเป็น 2.4 เปอร์เซ็นต์ของเปลือกโลก เนื่องจากปฏิกิริยาที่แข็งแกร่งของมันจึงไม่เกิดขึ้นในสถานะดั้งเดิม แต่จะพบได้ในสารประกอบที่หลากหลายในทะเลน้ำเค็มน้ำเค็มและหิน
ในบรรดาแร่แร่แร่ที่พบมากที่สุดคือ dolomite คาร์บอเนต (สารประกอบของแมกนีเซียมและแคลเซียมคาร์บอเนต MgCO 3 · CaCO 3) และ magnesite (แมกนีเซียมคาร์บอเนต MgCO 3) ที่พบได้น้อยคือไฮดรอกไซแร่บรูไซต์ Mg (OH) 2และคาร์นิวัลแร่เฮไลด์ (สารประกอบของแมกนีเซียมและโพแทสเซียมคลอไรด์และน้ำ MgCl 2 · KCl · 6H 2 O)
แมกนีเซียมคลอไรด์สามารถกู้คืนได้จากน้ำเกลือที่เกิดขึ้นตามธรรมชาติเช่น Great Salt Lake (โดยทั่วไปประกอบด้วยแมกนีเซียมร้อยละ 1.1 โดยน้ำหนัก) และทะเลเดดซี (3.4 เปอร์เซ็นต์) แต่ที่มาที่ใหญ่ที่สุดคือมหาสมุทรของโลก แม้ว่าน้ำทะเลจะมีแมกนีเซียมเพียงประมาณร้อยละ 0.13 แต่ก็แสดงถึงแหล่งที่ไม่สิ้นสุด
การขุดและการตั้งสมาธิ
ทั้งโดโลไมต์และแม็กเนไซต์ถูกขุดและเข้มข้นด้วยวิธีการทั่วไป Carnallite ถูกขุดขึ้นมาเป็นแร่หรือแยกออกจากสารประกอบเกลืออื่น ๆ ที่ถูกนำขึ้นสู่ผิวน้ำโดยการทำเหมืองสารละลาย น้ำเกลือที่มีแมกนีเซียมเกิดขึ้นตามธรรมชาตินั้นมีความเข้มข้นในบ่อน้ำขนาดใหญ่โดยการระเหยจากแสงอาทิตย์
การสกัดและการกลั่น
รีเอเจนต์ทางเคมีที่แข็งแกร่งแมกนีเซียมจะสร้างสารประกอบที่เสถียรและทำปฏิกิริยากับออกซิเจนและคลอรีนทั้งในสถานะของเหลวและก๊าซ ซึ่งหมายความว่าการสกัดโลหะจากวัตถุดิบเป็นกระบวนการที่ใช้พลังงานสูงซึ่งต้องใช้เทคโนโลยีที่ได้รับการปรับแต่งมาอย่างดี การผลิตเชิงพาณิชย์ใช้สองวิธีที่แตกต่างกันอย่างสมบูรณ์: อิเล็กโทรไลซิสของแมกนีเซียมคลอไรด์หรือการลดความร้อนของแมกนีเซียมออกไซด์ผ่านกระบวนการ Pidgeon อิเล็กโทรไลซิสมีสัดส่วนประมาณ 75 เปอร์เซ็นต์ของการผลิตแมกนีเซียมของโลก อย่างไรก็ตามในช่วงต้นศตวรรษที่ 21 เมื่อจีนกลายเป็นผู้ผลิตแมกนีเซียมชั้นนำของโลกต้นทุนแรงงานและพลังงานที่ต่ำทำให้กระบวนการ Pidgeon มีประสิทธิภาพทางเศรษฐกิจแม้ว่าจะมีประสิทธิภาพน้อยกว่าอิเล็กโทรไลซิสก็ตาม
กระแสไฟฟ้า
กระบวนการอิเล็กโทรไลติกประกอบด้วยสองขั้นตอน: การเตรียมวัตถุดิบที่ประกอบด้วยแมกนีเซียมคลอไรด์และการแยกตัวของสารประกอบนี้เป็นโลหะแมกนีเซียมและก๊าซคลอรีนในเซลล์อิเล็กโทรไลต์
ในกระบวนการอุตสาหกรรมฟีดของเซลล์ประกอบด้วยเกลือหลอมเหลวหลายชนิดที่มีแมกนีเซียมคลอไรด์ที่ปราศจากน้ำ (ส่วนใหญ่ปราศจากน้ำ), แมกนีเซียมคลอไรด์ที่ขาดน้ำบางส่วนหรือคาร์นิวัลที่ปราศจากน้ำ เพื่อหลีกเลี่ยงสิ่งเจือปนที่มีอยู่ในแร่ Carnallite แร่ Carnallite ประดิษฐ์ที่ไม่ผ่านการอบแห้งนั้นผลิตโดยการตกผลึกแบบควบคุมจากสารละลายแมกนีเซียมที่มีความร้อนและสารละลายที่มีโพแทสเซียม แมกนีเซียมคลอไรด์ที่ผ่านการอบแห้งบางส่วนนั้นสามารถรับได้จากกระบวนการ Dow ซึ่งน้ำทะเลผสมอยู่ในเครื่องจับตัวเป็นก้อนกับโดโลไมต์ปฏิกิริยาที่เผาไหม้เบา ๆ แมกนีเซียมไฮดรอกไซด์ที่ไม่ละลายน้ำจะตกตะกอนที่ด้านล่างของถังตกตะกอนซึ่งจะถูกสูบเป็นสารละลายกรองแล้วเปลี่ยนเป็นแมกนีเซียมคลอไรด์โดยทำปฏิกิริยากับกรดไฮโดรคลอริกและทำให้แห้งในขั้นตอนการระเหยถึง 25 เปอร์เซ็นต์ปริมาณน้ำ การคายน้ำขั้นสุดท้ายเกิดขึ้นในระหว่างการหลอม
แมกนีเซียมคลอไรด์รัสปราศจากการผลิตโดยสองวิธีหลัก: การคายน้ำของเกลือคลอไรด์แมกนีเซียมหรือคลอไรด์ของแมกนีเซียมออกไซด์ ในวิธีการหลังสุดขั้วโดยกระบวนการ IG Farben โดโลไมต์ที่ถูกเผาเบา ๆ ผสมกับน้ำทะเลในเครื่องจับตัวเป็นก้อนซึ่งแมกนีเซียมไฮดรอกไซด์จะถูกตกตะกอนกรองและเผาเพื่อแมกนีเซียมออกไซด์ ผสมกับถ่านก่อตัวเป็นกลมด้วยการเติมสารละลายแมกนีเซียมคลอไรด์และทำให้แห้ง ก้อนกลมจะถูกชาร์จเข้าไปในเครื่องคลอรีนซึ่งเป็นเตาเผาแบบมีอิฐเรียงรายซึ่งพวกมันจะถูกทำให้ร้อนด้วยอิเลคโทรดคาร์บอนจนถึงประมาณ 1,000–1,200 ° C (1,800–2,200 ° F) ก๊าซคลอรีนที่แนะนำผ่านช่องหน้าต่างในเตาทำปฏิกิริยากับแมกนีเซียมออกไซด์ในการผลิตแมกนีเซียมคลอไรด์ที่หลอมเหลวซึ่งจะถูกทาบทามเป็นระยะและส่งไปยังเซลล์อิเล็กโทรไลต์
การคายน้ำของน้ำเกลือแมกนีเซียมจะดำเนินการในขั้นตอน ในกระบวนการ Norsk Hydro สิ่งสกปรกจะถูกลบออกครั้งแรกโดยการเร่งรัดและการกรอง น้ำเกลือที่บริสุทธิ์ซึ่งมีแมกนีเซียมประมาณ 8.5 เปอร์เซ็นต์นั้นมีความเข้มข้นโดยการระเหยเป็น 14 เปอร์เซ็นต์และถูกเปลี่ยนเป็นอนุภาคในหอการฉายภาพ ผลิตภัณฑ์นี้ถูกทำให้แห้งไปยังอนุภาคที่ไม่มีน้ำและส่งไปยังเซลล์อิเล็กโทรไลต์
เซลล์อิเล็กโทรไลติกเป็นภาชนะที่มีอิฐเรียงรายไปด้วยแคโทดเหล็กและขั้วบวกกราไฟท์ สิ่งเหล่านี้จะถูกติดตั้งในแนวตั้งผ่านหน้ากากเซลล์และบางส่วนจมอยู่ในอิเล็กโทรไลต์เกลือหลอมเหลวที่ประกอบด้วยอัลคาไลน์คลอไรด์ซึ่งแมกนีเซียมคลอไรด์ที่ผลิตในกระบวนการที่อธิบายข้างต้นจะถูกเพิ่มในความเข้มข้น 6 ถึง 18 เปอร์เซ็นต์ ปฏิกิริยาพื้นฐานคือ:
อุณหภูมิในการทำงานจะแตกต่างกันไปจาก 680 ถึง 750 ° C (1,260 ถึง 1,380 ° F) การใช้พลังงาน 12 ถึง 18 กิโลวัตต์ชั่วโมงต่อการผลิตแมกนีเซียม คลอรีนและก๊าซอื่น ๆ จะถูกสร้างขึ้นที่ขั้วบวกของกราไฟท์และโลหะแมกนีเซียมหลอมเหลวจะลอยขึ้นไปด้านบนของอ่างเกลือซึ่งจะถูกเก็บรวบรวม คลอรีนสามารถนำกลับมาใช้ใหม่ได้ในกระบวนการอบแห้ง
ลดความร้อน
ในการผลิตความร้อนโดโลไมต์ถูกเผาเพื่อแมกนีเซียมออกไซด์ (MgO) และมะนาว (CaO) และเหล่านี้จะลดลงโดยซิลิคอน (Si) ยอมให้ก๊าซแมกนีเซียมและตะกรันของ dicalcium ซิลิเกต ปฏิกิริยาพื้นฐาน
คือความร้อน - นั่นคือต้องใช้ความร้อนเพื่อเริ่มต้นและรักษาความร้อน ด้วยแมกนีเซียมถึงความดันไอของ 100 kilopascals (1 บรรยากาศ) ที่ 1,800 ° C (3,270 ° F) ความต้องการความร้อนจึงค่อนข้างสูง เพื่อลดอุณหภูมิของปฏิกิริยาปฏิกิริยากระบวนการอุตสาหกรรมทำงานภายใต้สูญญากาศ มีวิธีการสามวิธีหลักซึ่งแตกต่างกันโดยวิธีการของพวกเขาในการจัดหาความร้อน ในกระบวนการ Pidgeon โดโลไมต์ที่บดและดินผสมกับเฟอโรซิลิกส์ที่บดละเอียดแล้วอัดเป็นก้อนและถูกอัดเข้าไปในเหล็กทรงกระบอกนิกเกิล - โครเมียม จำนวนการติดตั้งโต้กลับในแนวนอนในเตาเผาน้ำมันหรือก๊าซที่มีฝาปิดและระบบคอนเดนเซอร์ที่ยื่นออกมาจากเตา หลังจากรอบการเกิดปฏิกิริยาที่อุณหภูมิ 1,200 ° C (2,200 ° F) และภายใต้ความกดดันที่ลดลงจาก 13 pascals ผลึกแมกนีเซียม (เรียกว่าครอบฟัน) จะถูกลบออกจากเครื่องควบแน่น slag จะถูกอพยพออกมาเป็นของแข็งและจะถูกอัดประจุใหม่ ในกระบวนการโบลซาโน briquettes โดโลไมต์ - เฟอโรซิลิกส์จะถูกวางซ้อนกันบนระบบสนับสนุนการเก็บประจุพิเศษซึ่งจะนำเครื่องทำความร้อนไฟฟ้าภายในไปใช้กับประจุ ปฏิกิริยาที่สมบูรณ์ใช้เวลา 20 ถึง 24 ชั่วโมงที่ 1,200 ° C ต่ำกว่า 400 pascals
ตะกรัน dicalcium ซิลิเกตที่ผลิตโดยกระบวนการข้างต้นมีจุดหลอมเหลวประมาณ 2,000 ° C (3,600 ° F) ดังนั้นจึงอยู่ในสถานะของแข็ง แต่ด้วยการเติมอะลูมินา (อะลูมิเนียมออกไซด์ Al 2 O 3) ลงในประจุ จุดหลอมเหลวสามารถลดลงได้ถึง 1,550–1,600 ° C (2,825–2,900 ° F) เทคนิคนี้ใช้ในกระบวนการ Magnetherm มีความได้เปรียบที่ตะกรันเหลวสามารถให้ความร้อนโดยตรงโดยกระแสไฟฟ้าผ่านอิเล็กโทรดทองแดงที่ระบายความร้อนด้วยน้ำ ปฏิกิริยาการลดเกิดขึ้นที่ 1,600 ° C และความดัน pascals 400–670 แมกนีเซียมที่ถูกทำให้กลายเป็นไอจะถูกควบแน่นในระบบแยกต่างหากที่ติดอยู่กับเครื่องปฏิกรณ์และตะกรันที่หลอมเหลวและเฟอโรซิลิกส์จะถูกเคาะเป็นระยะ ๆ









![ปฏิวัติอิหร่าน [2521-2522] ปฏิวัติอิหร่าน [2521-2522]](https://images.thetopknowledge.com/img/world-history/8/iranian-revolution-19781979.jpg)