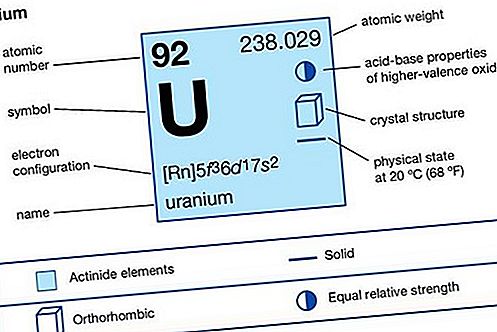
ยูเรเนียม (U)ซึ่งเป็นองค์ประกอบทางเคมีของสารกัมมันตรังสีของชุดแอคติโนนิดด์ของตารางธาตุเลขอะตอม 92 เป็นเชื้อเพลิงนิวเคลียร์ที่สำคัญ

องค์ประกอบ actinoid
สมาชิกของกลุ่มรวมถึงยูเรเนียม (ที่คุ้นเคยที่สุด) เกิดขึ้นตามธรรมชาติส่วนใหญ่เป็นสิ่งที่มนุษย์สร้างขึ้น มีการใช้ทั้งยูเรเนียมและพลูโตเนียม
ยูเรเนียมมีองค์ประกอบของเปลือกโลกประมาณสองส่วนต่อล้านส่วน แร่ยูเรเนียมที่สำคัญบางชนิด ได้แก่พิทบเลนด์(ไม่บริสุทธิ์ U 3 O 8), ยูโนนิก (UO 2), คาร์โนไทต์ (โพแทสเซียมยูเรเนียมวานาเดต), ออโตไนต์ (แคลเซียมยูเรเนียมฟอสเฟต) และ torbernite (ทองแดงยูเรเนียมฟอสเฟต) แร่ยูเรเนียมเหล่านี้และแร่อื่น ๆ ที่สามารถนำกลับมาใช้ใหม่ได้ซึ่งเป็นแหล่งเชื้อเพลิงนิวเคลียร์มีพลังงานมากกว่าเชื้อเพลิงฟอสซิลที่ได้รับคืนทั้งหมด ยูเรเนียมหนึ่งปอนด์ให้พลังงานมากถึง 1.4 ล้านกิโลกรัม (3 ล้านปอนด์) ของถ่านหิน
สำหรับข้อมูลเพิ่มเติมเกี่ยวกับการสะสมแร่ยูเรเนียมรวมถึงความครอบคลุมของการขุดการกลั่นและเทคนิคการกู้คืนดูการประมวลผลยูเรเนียม สำหรับข้อมูลสถิติเปรียบเทียบเกี่ยวกับการผลิตยูเรเนียมดูตาราง
ยูเรเนียม
| ประเทศ | ปริมาณการผลิตของปี 2556 (เมตริกตัน) | % ของการผลิตทุ่นระเบิดของโลก |
|---|---|---|
| * ประมาณการ | ||
| ที่มา: สมาคมนิวเคลียร์โลก, การผลิตเหมืองแร่ยูเรเนียมโลก (2014) | ||
| คาซัคสถาน | 22574 | 37.9 |
| แคนาดา | 9332 | 15.6 |
| ออสเตรเลีย | 6,350 | 10.6 |
| ไนเจอร์ * | 4528 | 7.6 |
| นามิเบีย | 4,315 | 7.2 |
| รัสเซีย | 3,135 | 5.3 |
| อุซเบกิ * | 2,400 | 4.0 |
| สหรัฐ | 1,835 | 3.1 |
| จีน * | 1,450 | 2.4 |
| มาลาวี | 1,132 | 1.9 |
| ยูเครน | 1,075 | 1.9 |
| แอฟริกาใต้ | 540 | 0.9 |
| อินเดีย* | 400 | 0.7 |
| สาธารณรัฐเช็ก | 225 | 0.4 |
| บราซิล | 198 | 0.3 |
| โรมาเนีย * | 80 | 0.1 |
| ปากีสถาน* | 41 | 0.1 |
| ประเทศเยอรมัน | 27 | 0.0 |
| รวมโลก | 59637 | 100 |
ยูเรเนียมเป็นองค์ประกอบที่ทำจากโลหะแข็งที่มีสีขาวเงิน มันมีความยืดหยุ่นอ่อนตัวและสามารถขัดเงาได้สูง ในอากาศทำให้เสื่อมเสียโลหะและเมื่อแบ่งออกอย่างประณีตแบ่งเป็นเปลวไฟ มันเป็นตัวนำไฟฟ้าที่ค่อนข้างแย่ แม้ว่าการค้นพบ (1789) โดยนักเคมีชาวเยอรมันมาร์ตินเฮ็น Klaproth ที่ตั้งชื่อมันหลังจากที่ดาวเคราะห์ที่แล้วเพิ่งค้นพบดาวยูเรนัสโลหะของตัวเองที่แยกได้เป็นครั้งแรก (1841) โดยนักเคมีชาวฝรั่งเศสยูจีนเมลชอร์เพลิ ก็อต จากการลดลงของยูเรเนียม tetrachloride นี้ (UCL 4) ด้วย โพแทสเซียม.
สูตรของระบบเคมีเป็นระยะโดยนักเคมีชาวรัสเซีย Dmitry Mendeleyev ในปี ค.ศ. 1869 มุ่งเน้นความสนใจไปที่ยูเรเนียมในฐานะองค์ประกอบทางเคมีที่หนักที่สุดซึ่งเป็นตำแหน่งที่จัดขึ้นจนกระทั่งค้นพบเนปจูนธาตุ transuranium ธาตุแรกในปี 1940 ในปี 1896 นักฟิสิกส์ชาวฝรั่งเศส ปรากฏการณ์ของกัมมันตภาพรังสีเป็นคำที่ใช้ครั้งแรกในปี 1898 โดยนักฟิสิกส์ชาวฝรั่งเศส Marie และ Pierre Curie คุณสมบัตินี้พบในภายหลังในองค์ประกอบอื่น ๆ อีกมากมาย ตอนนี้เป็นที่รู้จักกันว่ายูเรเนียมกัมมันตภาพรังสีในไอโซโทปทั้งหมดประกอบด้วยธรรมชาติของยูเรเนียม -238 (99.27 เปอร์เซ็นต์, ครึ่งชีวิต 4,510,000,000 ปี, ยูเรเนียม-235 (0.72 เปอร์เซ็นต์, ครึ่งชีวิต 713,000,000 ปี) และ ยูเรเนียม -234 (0.006 เปอร์เซ็นต์ครึ่งชีวิต 247,000 ปี) ครึ่งชีวิตที่ยาวนานเหล่านี้ทำให้การตรวจสอบอายุของโลกเป็นไปได้โดยการวัดปริมาณตะกั่วซึ่งเป็นผลิตภัณฑ์การสลายตัวขั้นสุดท้ายของยูเรเนียมในหินที่ประกอบด้วยยูเรเนียม ยูเรเนียม -238 เป็นพ่อแม่และยูเรเนียม -238 หนึ่งในลูกสาวในซีรีย์กัมมันตภาพรังสียูเรเนียม uranium-235 เป็นส่วนประกอบหลักของชุดการสลายตัวของแอกทิเนียม ดูองค์ประกอบ actinoid
ธาตุยูเรเนียมกลายเป็นเรื่องของการศึกษาที่เข้มข้นและความสนใจอย่างกว้างขวางหลังจากนักเคมีชาวเยอรมันอ็อตโตฮาห์นและฟริตซ์สตราสแมนน์ค้นพบในปลายปี 2481 ปรากฏการณ์การแตกตัวของนิวเคลียร์ในยูเรเนียม นักฟิสิกส์ชาวอเมริกันชาวอิตาเลียน Enrico Fermi แนะนำ (ต้นปี 1939) ว่านิวตรอนอาจเป็นหนึ่งในผลิตภัณฑ์ฟิชชันและอาจทำให้ฟิชชันดำเนินต่อไปในฐานะปฏิกิริยาลูกโซ่ นักฟิสิกส์ชาวอเมริกันที่เกิดในฮังการีลีโอซิลลาร์ดนักฟิสิกส์ชาวอเมริกันเฮอร์เบิร์ตแอนเดอร์สันนักเคมีชาวฝรั่งเศสFrédéric Joliot-Curie และเพื่อนร่วมงานของพวกเขายืนยัน (1939) คำทำนายนี้; การตรวจสอบภายหลังพบว่าค่าเฉลี่ยของ 2 1 / 2นิวตรอนต่ออะตอมจะถูกปล่อยออกในระหว่างการแบ่งเซลล์ การค้นพบเหล่านั้นนำไปสู่ปฏิกิริยาลูกโซ่นิวเคลียร์ที่ยั่งยืนด้วยตัวเองครั้งแรก (2 ธันวาคม 2485) การทดสอบระเบิดปรมาณูครั้งแรก (16 กรกฎาคม 2488) ระเบิดปรมาณูลูกแรกหล่นลงในสงคราม (6 สิงหาคม 2488) การขับเคลื่อนด้วยอะตอมครั้งแรก submarine (1955) และเครื่องกำเนิดไฟฟ้าพลังงานนิวเคลียร์เต็มรูปแบบเครื่องแรก (1957)
ฟิชชันเกิดขึ้นกับนิวตรอนช้าในไอโซโทปยูเรเนียม -235 ที่หายาก (ซึ่งเป็นวัสดุฟิสไซล์ที่เกิดขึ้นเองตามธรรมชาติ) ซึ่งจะต้องแยกออกจากไอโซโทปยูเรเนียม -238 ที่อุดมสมบูรณ์สำหรับการใช้งานที่หลากหลาย อย่างไรก็ตามยูเรเนียม -238 นั้นหลังจากดูดซับนิวตรอนและผ่านการสลายตัวของบีตาแบบลบจะถูกส่งไปยังพลูโทเนียมที่เป็นองค์ประกอบสังเคราะห์ซึ่งเป็นฟิชไซล์ที่มีนิวตรอนช้า ดังนั้นยูเรเนียมธรรมชาติจึงสามารถใช้ในเครื่องปฏิกรณ์แปลงและเครื่องปฏิกรณ์พ่อแม่พันธุ์ซึ่งมีการแยกเซลล์โดยยูเรเนียม - 235 ที่หายากและพลูโทเนียมผลิตขึ้นในเวลาเดียวกันโดยการเปลี่ยนรูปของยูเรเนียม -238 Fissile uranium-233 สามารถสังเคราะห์ขึ้นเพื่อใช้เป็นเชื้อเพลิงนิวเคลียร์จากไอโซโทปทอเรียมไม่ทอเรียมทอเรียม -232 ซึ่งมีมากมายในธรรมชาติ ยูเรเนียมก็มีความสำคัญเช่นเดียวกับวัสดุหลักซึ่งองค์ประกอบของทรานเฟอร์เรียมสังเคราะห์ได้ถูกจัดทำขึ้นโดยปฏิกิริยาการเปลี่ยนรูป
ยูเรเนียมซึ่งเป็นอิเล็กโตรโพสิทีฟตัวทำปฏิกิริยากับน้ำ มันละลายในกรด แต่ไม่เป็นด่าง สถานะออกซิเดชันที่สำคัญคือ +4 (เช่นในออกไซด์ UO 2, tetrahalides เช่น UCl 4และไอออนน้ำสีเขียว U 4 +) และ +6 (เช่นเดียวกับออกไซด์ UO 3, hexafluoride UF 6, และ uranyl สีเหลือง ไอออน UO 2 2+) ในสารละลายแร่ยูเรเนียมที่มีเสถียรภาพมากที่สุดเป็นไอออน uranyl ซึ่งมีโครงสร้างเชิงเส้น [O = U = O] 2+ ยูเรเนียมยังแสดงสถานะเป็น +3 และ +5 แต่ไอออนนั้นไม่เสถียร ไอออนสีแดง U 3+ จะออกซิไดซ์อย่างช้าๆแม้ในน้ำที่ไม่มีออกซิเจนละลาย สีของไอออนUO 2 +ไม่เป็นที่รู้จักเพราะมันผ่านการแยกส่วน (UO 2 +จะลดลงเป็น U 4 +และออกซิไดซ์เป็น UO 2 2+) แม้ในสารละลายเจือจางมาก
สารประกอบยูเรเนียมถูกใช้เป็นสารช่วยสีสำหรับเซรามิกส์ ยูเรเนียมเฮกซาฟลูออไรด์ (UF 6) เป็นของแข็งที่มีความดันไอสูงผิดปกติ (115 torr = 0.15 atm = 15,300 Pa) ที่ 25 ° C (77 ° F) UF 6นั้นมีปฏิกิริยาทางเคมีมาก แต่ถึงแม้จะมีฤทธิ์กัดกร่อนในสถานะไอ แต่ UF 6นั้นถูกนำมาใช้กันอย่างแพร่หลายในการแพร่กระจายของก๊าซและวิธีการหมุนเหวี่ยงด้วยแก๊สในการแยกยูเรเนียม -235 จากยูเรเนียม -238
สารประกอบออร์แกโนเมทัลลิกเป็นสารประกอบที่น่าสนใจและสำคัญซึ่งมีพันธะโลหะ - คาร์บอนเชื่อมโยงโลหะกับกลุ่มอินทรีย์ Uranocene เป็นสารประกอบ organouranium U (C 8 H 8) 2ซึ่งในอะตอมยูเรเนียมคั่นกลางระหว่างสองชั้นแหวนอินทรีย์ที่เกี่ยวข้องกับ cyclooctatetraene C 8 H 8 การค้นพบของมันในปี 1968 ได้เปิดสาขาเคมีออร์กาเมติกแบบใหม่
คุณสมบัติองค์ประกอบ
| เลขอะตอม | 92 |
|---|---|
| น้ำหนักปรมาณู | 238.03 |
| จุดหลอมเหลว | 1,132.3 ° C (2,070.1 ° F) |
| จุดเดือด | 3,818 ° C (6,904 ° F) |
| แรงดึงดูดเฉพาะ | 19.05 |
| สถานะออกซิเดชัน | +3, +4, +5, +6 |
| การกำหนดค่าอิเล็กตรอนของสถานะอะตอมของก๊าซ | [Rn] 5f 3 6d 1 7 วินาที2 |