ฮีเลียม (เขา)องค์ประกอบทางเคมีก๊าซเฉื่อยของกลุ่ม 18 (ก๊าซมีตระกูล) ของตารางธาตุ องค์ประกอบที่เบาที่สุดที่สอง (ไฮโดรเจนเท่านั้นที่มีน้ำหนักเบา) ฮีเลียมเป็นก๊าซไม่มีสีไม่มีกลิ่นและไร้รสซึ่งกลายเป็นของเหลวที่ − 268.9 ° C (−452 ° F) จุดเดือดและจุดเยือกแข็งของฮีเลียมต่ำกว่าสารอื่นที่รู้จัก ฮีเลียมเป็นองค์ประกอบเดียวที่ไม่สามารถทำให้เป็นก้อนโดยการระบายความร้อนที่เพียงพอที่ความดันบรรยากาศปกติ จำเป็นต้องใช้แรงดัน 25 บรรยากาศที่อุณหภูมิ 1 K (−272 ° C หรือ −458 ° F) เพื่อแปลงให้อยู่ในรูปของแข็ง
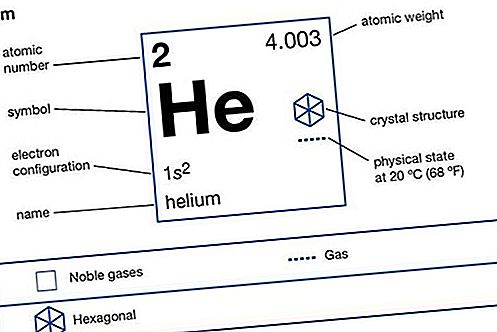

ก๊าซมีตระกูล
องค์ประกอบคือฮีเลียม (He), นีออน (Ne), อาร์กอน (Ar), คริปทอน (Kr), ซีนอน (Xe), เรดอน (Rn) และ oganesson (Og) ก๊าซมีตระกูลต่าง ๆ
คุณสมบัติองค์ประกอบ
| เลขอะตอม | 2 |
|---|---|
| น้ำหนักปรมาณู | 4.0026 |
| จุดหลอมเหลว | ไม่มี |
| จุดเดือด | −268.9 ° C (−452 ° F) |
| ความหนาแน่น (1 atm, 0 ° C) | 0.1785 กรัม / ลิตร |
| สถานะออกซิเดชัน | 0 |
| การกำหนดค่าอิเล็กตรอน | 1 วินาที2 |
ประวัติศาสตร์
ฮีเลียมถูกค้นพบในบรรยากาศก๊าซรอบดวงอาทิตย์โดยนักดาราศาสตร์ชาวฝรั่งเศสปิแอร์แจนเซ่นซึ่งตรวจพบเส้นสีเหลืองสดใสในสเปกตรัมของ chromosphere สุริยะในช่วงที่เกิดคราส 2411; บรรทัดนี้ในขั้นต้นสันนิษฐานว่าเป็นตัวแทนขององค์ประกอบโซเดียม ในปีเดียวกันนั้นนักดาราศาสตร์อังกฤษโจเซฟนอร์แมนอคเยอร์สังเกตเห็นเส้นสีเหลืองในสเปกตรัมแสงอาทิตย์ที่ไม่สอดคล้องกับที่รู้จักกัน D 1และ D 2เส้นของโซเดียมและเพื่อให้เขาตั้งชื่อมันว่า D 3บรรทัด ลอคเยอร์สรุปว่าเส้น D 3นั้นเกิดจากธาตุในดวงอาทิตย์ที่ไม่เป็นที่รู้จักบนโลก เขาและนักเคมีเอ็ดเวิร์ดแฟรงค์แลนด์ใช้คำกรีกสำหรับดวงอาทิตย์hēliosในการตั้งชื่อองค์ประกอบ นักเคมีชาวอังกฤษ Sir William Ramsay ค้นพบการมีอยู่ของฮีเลียมบนโลกในปี 1895 Ramsay ได้รับตัวอย่างของ cleveite แร่แบริ่งยูเรเนียมและเมื่อตรวจสอบก๊าซที่ผลิตโดยการให้ความร้อนตัวอย่างเขาพบว่าเส้นสีเหลืองสดใสที่ไม่ซ้ำกัน สเปกตรัมที่ตรงกับของเส้น D 3 ที่สังเกตในสเปกตรัมของดวงอาทิตย์ องค์ประกอบใหม่ของฮีเลียมจึงถูกระบุอย่างชัดเจน ในปี 1903 Ramsay และ Frederick Soddy ได้กำหนดเพิ่มเติมว่าฮีเลียมเป็นผลมาจากการสลายตัวโดยธรรมชาติของสารกัมมันตรังสี
ความอุดมสมบูรณ์และไอโซโทป
ฮีเลียมประกอบด้วยมวลประมาณ 23 เปอร์เซ็นต์ของมวลของเอกภพดังนั้นจึงเป็นที่สองรองจากไฮโดรเจนในจักรวาล ฮีเลียมนั้นกระจุกตัวในดาวฤกษ์ซึ่งมันถูกสังเคราะห์จากไฮโดรเจนด้วยการหลอมนิวเคลียร์ แม้ว่าฮีเลียมจะเกิดขึ้นในชั้นบรรยากาศของโลกเพียง 1 ส่วนใน 200,000 (0.0005 เปอร์เซ็นต์) และมีปริมาณเล็กน้อยในแร่ธาตุกัมมันตรังสีเหล็กอุตุนิยมวิทยาและน้ำพุแร่ธาตุฮีเลียมจำนวนมากพบได้ในส่วนประกอบ (มากถึง 7.6 เปอร์เซ็นต์) ใน ก๊าซธรรมชาติในสหรัฐอเมริกา (โดยเฉพาะในเท็กซัส, นิวเม็กซิโก, แคนซัส, โอคลาโฮมา, แอริโซนา, และยูทาห์) อุปกรณ์ขนาดเล็กถูกค้นพบในแอลจีเรีย, ออสเตรเลีย, โปแลนด์, กาตาร์และรัสเซีย อากาศธรรมดามีฮีเลียมประมาณ 5 ส่วนต่อล้านส่วนเปลือกโลกโลกอยู่ที่ 8 ส่วนต่อพันล้านเท่านั้น
นิวเคลียสของอะตอมฮีเลียมทุกอันมีสองโปรตอน แต่ในกรณีที่มีธาตุทั้งหมดไอโซโทปของฮีเลียมจะมีอยู่ ไอโซโทปที่เป็นที่รู้จักของฮีเลียมนั้นประกอบด้วยนิวตรอนหนึ่งถึงหกตัวดังนั้นจำนวนมวลของพวกมันจึงอยู่ในช่วงสามถึงแปด ในหกไอโซโทปเหล่านี้มีเพียงไอโซโทปมวลสามตัว (ฮีเลียม -3 หรือ3ฮี) และสี่ (ฮีเลียม -4 หรือ4เขา) มีเสถียรภาพ อื่น ๆ ทั้งหมดนั้นมีกัมมันตภาพรังสีสลายอย่างรวดเร็วในสารอื่น ๆ ฮีเลียมที่มีอยู่บนโลกไม่ใช่องค์ประกอบหลัก แต่เกิดจากการสลายตัวของสารกัมมันตรังสี อนุภาคอัลฟ่าที่ถูกปล่อยออกมาจากนิวเคลียสของสารกัมมันตรังสีที่หนักกว่าคือนิวเคลียสของไอโซโทปฮีเลียม -4 ฮีเลียมไม่สะสมในชั้นบรรยากาศในปริมาณมากเพราะแรงโน้มถ่วงของโลกไม่เพียงพอที่จะป้องกันการหลบหนีอย่างค่อยเป็นค่อยไปสู่อวกาศ ร่องรอยของไอโซโทปฮีเลียม -3 บนโลกนั้นเป็นผลมาจากการสลายตัวของบีตาลบของไอโซโทปไฮโดรเจน -3 ที่หายาก (ไอโซโทป) ฮีเลียม -4 มีความเสถียรมากที่สุดของไอโซโทปเสถียร: ฮีเลียม -4 อะตอมมากกว่าฮีเลียม -3 ประมาณ 700,000: 1 ในฮีเลียมในบรรยากาศและประมาณ 7,000,000: 1 ในแร่ธาตุที่มีฮีเลียมบางตัว
คุณสมบัติ
ฮีเลียม -4 มีลักษณะพิเศษในการมีสองรูปแบบของเหลว รูปแบบของเหลวปกติเรียกว่าฮีเลียม 1 และอยู่ที่อุณหภูมิจากจุดเดือด 4.21 K (− 268.9 ° C) ลงไปประมาณ 2.18 K (−271 ° C) ต่ำกว่า 2.18 เคลวินค่าการนำความร้อนของฮีเลียม -4 มากกว่า 1,000 เท่าของทองแดง รูปแบบของเหลวนี้เรียกว่าฮีเลียม II เพื่อแยกความแตกต่างจากฮีเลียมเหลวปกติ I. ฮีเลียม II แสดงคุณสมบัติที่เรียกว่า superfluidity: ความหนืดหรือความต้านทานต่อการไหลของมันอยู่ในระดับต่ำจนไม่ได้วัด ของเหลวนี้แพร่กระจายในฟิล์มบางบนพื้นผิวของสารใด ๆ ที่มันสัมผัสและฟิล์มนี้จะไหลโดยไม่มีแรงเสียดทานแม้กับแรงโน้มถ่วง ในทางตรงกันข้ามฮีเลียม -3 ที่อุดมสมบูรณ์น้อยกว่านั้นจะสร้างเฟสของเหลวที่แตกต่างกันสามแบบซึ่งสองอันนั้นเป็น superfluids Superfluidity in helium-4 ถูกค้นพบโดย Pyotr Leonidovich Kapitsa นักฟิสิกส์ชาวรัสเซียในช่วงกลางทศวรรษ 1930 และปรากฎการณ์เดียวกันใน helium-3 ครั้งแรกโดย Douglas D. Osheroff, David M. Lee, และ Robert C. Richardson of the United อเมริกาในปี 1972

ส่วนผสมของเหลวของไอโซโทปฮีเลียม -3 และฮีเลียม -4 แยกกันที่อุณหภูมิต่ำกว่าประมาณ 0.8 K (− 272.4 ° C หรือ −458.2 ° F) เป็นสองชั้น ชั้นหนึ่งเป็นฮีเลียมบริสุทธิ์ในทางปฏิบัติ -3; ส่วนใหญ่เป็นฮีเลียม -4 แต่ยังคงฮีเลียม -3 ประมาณ 6 เปอร์เซ็นต์แม้ที่อุณหภูมิต่ำสุดที่ทำได้ การสลายตัวของฮีเลียม -3 ในฮีเลียม -4 นั้นมาพร้อมกับเอฟเฟกต์ความเย็นที่ใช้ในการก่อสร้าง cryostats (อุปกรณ์สำหรับการผลิตที่อุณหภูมิต่ำมาก) ที่สามารถบรรลุได้ - และคงไว้ซึ่งอุณหภูมิต่ำสุด 0.01 K (−273.14 ° C หรือ −459.65 ° F)






![ภาพยนตร์ Sullivan "Travels by Sturges [1941] ภาพยนตร์ Sullivan "Travels by Sturges [1941]](https://images.thetopknowledge.com/img/entertainment-pop-culture/1/sullivanquots-travels-film-sturges-1941.jpg)






